Часть 2.4.Отчет о результатах методического анализа результатов ЕГЭ по химии
1.Характеристика участников ЕГЭ
Количество участников ЕГЭ за 3 года:
Таблица 105
| Предмет | 2013 | 2014 | 2015 | |||
| чел. | % от общего числа участников | чел. | % от общего числа участников | чел. | % от общего числа участников | |
| Химия | 1074 | 15,2 | 961 | 16,16 | 956 | 16,63 |
Юношей и девушек:
Таблица 106
| Пол | Участников всего | Участников | Средний балл |
| Юноши | 2900 | 277 | 49,9 |
| Девушки | 2955 | 679 | 50,86 |
| Итого по КБР | 5855 | 956 | 50,58 |
Количество участников ЕГЭ в регионе по категориям
Таблица 107
| Всего участников ЕГЭ по предмету | Химия |
| Из них: | 956 |
| Выпускников текущего года | 904 |
| Выпускников СПО | 6 |
| Выпускников прошлых лет | 50 |
Количество участников по типам ОО
Таблица 108
| Всего участников ЕГЭ по предмету | Химия |
| Из них: | 956 |
| Выпускники лицеев и гимназий | 147 |
| Выпускники СОШ | 687 |
Количество участников ЕГЭ по химии по административным образованиям региона
Таблица 109
| АТЕ | Количество участников по предмету | в % к общему числу выпускников |
| Нальчик | 337 | 5,7 |
| Баксан | 68 | 1,2 |
| Прохладный | 40 | 0,7 |
| Баксанский район | 119 | 2 |
| Зольский район | 45 | 0,8 |
| Лескенский район | 28 | 0,5 |
| Майский район | 34 | 0,6 |
| Прохладненский район | 27 | 0,5 |
| Терский район | 54 | 0,9 |
| Урванский район | 76 | 1,2 |
| Чегемский район | 55 | 0,9 |
| Черекский район | 37 | 0,7 |
| Эльбрусский район | 36 | 0,7 |
2.Краткая характеристика КИМ по химии
КИМы составлены на основе спецификации КИМ ЕГЭ по химии, задания охватывают все элементы, которые приведены в кодификаторе элементов содержания и требований к уровню подготовки выпускников образовательных организаций для проведения ЕГЭ по химии. Количество вариантов КИМ достаточно (10 в основном потоке и 2 в резервном). Вопросы составлены по разделам и с учетом сложности. В целом необходимости в совершенствовании КИМ ЕГЭ по химии нет.
3.Основные результаты ЕГЭ по предмету
3.1.В текущем году
Средний балл ЕГЭ по химии в регионе - 51
Основные результаты:
Таблица 110
| Химия | Количество | В % к общему числу участников ЕГЭ по предмету |
| Доля участников, набравших баллов ниже минимального значения | 178 | 18,6 |
| Количество (доля) участников, получивших от 81 до 100 баллов | 46 | 4,8 |
| Количество выпускников, получивших 100 баллов | 2 | 0,2 |
Результаты по категориям участников ЕГЭ :
Таблица 111
| Химия | Выпускники организаций среднего общего образования | Выпускники СПО | Выпускники прошлых лет |
| Доля участников, набравших баллов ниже минимального значения | 17 | 66,6 | 43,5 |
| Средний балл | 51,4 | 30,8 | 36,1 |
| Доля участников, получивших от 81 до 100 баллов | 5,1 | 0 | 0 |
| Количество выпускников, получивших 100 баллов | 2 | 0 | 0 |
Результаты по кластерам ОО:
Таблица 112
| Химия | СОШ | Гимназии, лицеи |
| Доля участников, набравших баллов ниже минимального значения | 18,5 | 9,1 |
| Средний балл | 50 | 59,1 |
| Доля участников, получивших от 81 до 100 баллов | 4 | 11,1 |
| Количество выпускников, получивших 100 баллов | 0 | 2 |
3.2.Динамика результатов ЕГЭ по предмету за последние 2-3 года
Таблица 113
| Химия | КБР | ||
| ЕГЭ-2013 | ЕГЭ-2014 | ЕГЭ-2015 | |
| Не преодолели минимальной границы | 22 | 233 | 178 |
| Средний балл | 72,3 | 40,6 | 50.58 |
| Набрали от 81 до 100 баллов | 310 | 28 | 46 |
| Получили 100 баллов | 0 | 2 | 2 |
3.3.Основные результаты ЕГЭ по химии в сравнении
по административно территориальным единицам
Таблица 114
| АТЕ | По не преодолевшим минимальную границу | По среднему баллу | По высокобальникам(от81-100 баллов) |
| Нальчик | 21,07 | 51,89 | 7,4 |
| Прохладный | 15 | 60,15 | 12,5 |
| Баксан | 25 | 47,01 | 2,9 |
| Баксанский район | 17,65 | 46,83 | 1,7 |
| Зольский район | 20 | 45,69 | 0 |
| Лескенский район | 10,71 | 45,86 | 0 |
| Майскому району | 11,76 | 53,18 | 2,9 |
| Прохладненский район | 22,22 | 45,15 | 0 |
| Терский район | 5,56 | 58,5 | 7,4 |
| Урванский район | 14,47 | 53,13 | 5,3 |
| Чегемский район | 30,91 | 44,47 | 0 |
| Черекский район | 8,11 | 52,86 | 0 |
| Эльбрусский район | 19,44 | 47,86 | 2,8 |
4.Анализ результатов выполнения отдельных заданий или групп заданий.
Новое в структуре контрольно-измерительных материалов (КИМов) по химии в целом положительно отразилось на результатах выполнения заданий первой части (форма 1). Необходимо отметить, что выполнение заданий повышенного и высокого уровней сложности (часть I и часть II) вызывают затруднения у большинства выпускников (приложения форма 1,2,20). Наибольшие затруднения вызвали задания 38 (С3) и 40 (С5) из высокого уровня (форма 1), а из заданий повышенного уровня – 30-32, 34 и 35 (форма 1,2, см. таблицы и диаграммы).
Два выпускника в этом году показали высший результат. Анализ ответов обучающихся на задания с развернутым ответом в первую очередь указывает на ошибки и неточности при составлении уравнений химических реакций (неорганических и органических веществ). Возможная причина получения выявленных типичных ошибочных ответов является небольшая практика занятий по составлению уравнений химических реакций с использованием генетической взаимосвязи неорганических и (или) органических веществ, а также решения расчетных задач и составлений структурных формул органических веществ.
Задания и проверяемые ими элементы содержания, умения и способы деятельности, усвоение которых выпускниками в целом можно считать достаточными.
Для повышения уровня знаний и соответственно ответов обучающихся необходимо увеличить внимание и время на практические занятия, связанные с изучением генетической взаимосвязи между веществами различных классов (неорганических и (или) органических веществ) путем составления соответствующих реакций с учетом заданных условий их проведения, а также проводить расчеты по уравнению (или схеме) химической реакции. Проводить дополнительные занятия: качественные реакции на неорганические вещества и ионы; идентификация органических соединений; классификация и номенклатура неорганических веществ органических соединений; гидролиз солей; характерные химические свойства неорганических веществ и органических соединений; нахождение молекулярной и структурной формулы вещества.
Статистика ответов на вопросы ЕГЭ по химии
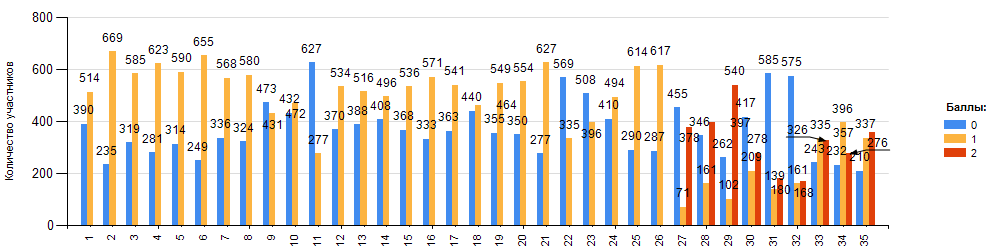
Порядковые номера заданий в работе: 1–26 – задания базового уровня сложности, с кратким ответом; 27–35 – задания повышенного уровня сложности, с кратким ответом; 36–40 – задания высокого уровня сложности, с развёрнутым ответом.
Обозначение уровня сложности заданий: Б – базовый уровень сложности;
П – повышенный уровень сложности; В – высокий уровень сложности.
Таблица 115
|
Порядковый номер задания в работе |
Проверяемые элементы содержания |
Коды прове-ряемых элементов содержа-ния по кодифи-катору |
Коды требований |
Уровень слож-ности зада- ния |
Средний процент выполнения по региону |
|
1 |
Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атома. Основное и возбужденное состояние атомов |
1.1.1 |
1.2.1 2.3.1 |
Б | 56,86 |
|
2 |
Закономерности изменения химических свойств элементов и их соединений по периодам и группам Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менде-леева и особенностями строения их атомов. Характеристика переходных элементов – меди, цинка, хрома, железа – по их положению в Периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов. Общая характеристика неметаллов IVА–VIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менде-леева и особенностями строения их атомов |
1.2.1 1.2.2 1.2.3 1.2.4 |
1.2.3 2.4.1 2.3.1 |
Б |
74 |
|
3 |
Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь | 1.3.1 |
2.2.2 2.4.2 |
Б | 64,71 |
|
4 |
Электроотрицательность. Степень окисления и валентность химических элементов | 1.3.2 |
1.1.1 2.2.1 |
Б | 68,92 |
|
5 |
Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения | 1.3.3 |
2.2.2 2.4.3 |
Б | 65,27 |
|
6 |
Классификация неорганических веществ. Номенклатура неорганических веществ (тривиаль-ная и международная). Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная) |
2.1 3.3 |
1.3.1 2.2.6 |
Б | 72,46 |
|
7 |
Характерные химические свойства простых веществ-металлов: щелочных, щелочноземельных, алюминия; переходных металлов: меди, цинка, хрома, железа. Характерные химические свойства простых веществ-неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния |
2.2 2.3 |
2.3.2 | Б | 62,83 |
|
8 |
Характерные химические свойства оксидов: оснóвных, амфотерных, кислотных | 2.4 | 2.3.3 | Б | 64,16 |
|
9 |
Характерные химические свойства оснований и амфотерных гидроксидов. Характерные химические свойства кислот |
2.5 2.6 |
2.3.3 | Б | 47,68 |
|
10 |
Характерные химические свойства солей: средних, кислых, оснóвных; комплексных (на примере соединений алюминия и цинка) | 2.7 | 2.3.3 | Б | 52,21 |
|
11 |
Взаимосвязь неорганических веществ | 2.8 |
2.3.3 2.4.3 |
Б | 30,64 |
|
12 |
Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах. Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа |
3.1 3.2 |
1.2.1 1.2.2 2.2.3 2.2.7 |
Б | 59,07 |
|
13 |
Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола) | 3.4 |
2.3.4 |
Б | 57,08 |
|
14 |
Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола | 3.5 | 2.3.4 | Б | 54,87 |
|
15 |
Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров. Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды, полисахариды) |
3.6 | 2.3.4 | Б | 59,29 |
|
16 |
Основные способы получения углеводородов (в лаборатории). Основные способы получения кислородсодержащих соединений |
4.1.7 4.1.8 |
1.3.4 2.5.1 |
Б | 63,16 |
|
17 |
Взаимосвязь углеводородов и кислородсодержащих органических соединений | 3.9 |
2.3.4 2.4.3 |
Б | 59,85 |
|
18 |
Классификация химических реакций в неорганической и органической химии | 1.4.1 | 2.2.8 | Б | 51,33 |
|
19 |
Скорость реакции, ее зависимость от различных факторов | 1.4.3 | 2.4.5 | Б | 60,73 |
|
20 |
Обратимые и необратимые химические реакции. Химическое равновесие. Смещение равновесия под действием различных факторов | 1.4.4 | 2.4.5 | Б | 61,28 |
|
21 |
Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты. Реакции ионного обмена |
1.4.5 1.4.6 |
1.1.1 1.1.2 1.2.1 2.4.4 |
Б |
69,36 |
|
22 |
Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии. Научные методы исследования химических веществ и превращений. Методы разделения смесей и очистки веществ. Качественные реакции на неорганические вещества и ионы. Идентификация органических соединений |
4.1.1 4.1.2 4.1.4 4.1.5 |
1.3.2 2.2.4 2.5.1 |
Б | 37,06 |
|
23 |
Понятие о металлургии: общие способы получения металлов. Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружа-ющей среды и его последствия. Природные источники углеводородов, их переработка. Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки |
4.2.1 4.2.2 4.2.3 4.2.4 |
1.3.3 1.3.4 |
Б | 43,81 |
|
24 |
Вычисление массы растворенного вещества, содержащегося в определенной массе раствора с известной массовой долей; вычисление массовой доли вещества в растворе | 4.3.1 | 2.5.2 | Б | 54,65 |
|
25 |
Расчеты объемных отношений газов при химических реакциях. Тепловой эффект химической реакции. Термохимические уравнения. Расчеты теплового эффекта реакции |
4.3.2 4.3.4 |
2.5.2 | Б | 67,92 |
|
26 |
Расчеты массы вещества или объ-ема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ | 4.3.3 | 2.5.2 | Б | 68,25 |
|
27 |
Классификация неорганических веществ. Классификация и номенклатура органических соединений |
2.1 3.3 |
2.2.8 | П | 41,81 |
|
28 |
Электроотрицательность. Степень окисления и валентность химических элементов. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее |
1.3.2 1.4.8 |
2.2.1 2.2.5 |
П | 43,92 |
|
29 |
Электролиз расплавов и растворов (солей, щелочей, кислот) | 1.4.9 |
1.1.3 2.2.5 |
П | 59,73 |
|
30 |
Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная |
1.4.7 | 2.2.4 | П | 30,75 |
|
31 |
Характерные химические свойства неорганических веществ: – простых веществ – металлов: щелочных, щелочноземельных, алюминия, переходных металлов (меди, цинка, хрома, железа); – простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния; – оксидов: оснóвных, амфотерных, кислотных; – оснований и амфотерных гидроксидов; – кислот; – солей: средних, кислых, оснóвных; комплексных (на примере соединений алюминия и цинка) |
2.2 2.3 2.4 2.5 2.6 2.7 |
2.3.3 | П | 19,91 |
|
32 |
Качественные реакции на неорганические вещества и ионы. Качественные реакции органических соединений |
4.1.4 4.1.5 |
2.5.1 2.2.4 |
П | 18,58 |
|
33 |
Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и толуола). Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии |
3.4 1.4.10 |
2.3.4 2.4.4 |
П | 36,06 |
|
34 |
Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола, альдегидов, предельных карбоновых кислот, сложных эфиров |
3.5 3.6 |
2.3.4 | П | 30,53 |
|
35 |
Характерные химические свойства азотсодержащих органических соединений: амиинов и аминокислот. Биологически важные вещества: жиры, углеводы (моносахариды, дисахариды, полисахариды), белки |
3.7 3.8 |
2.3.4 | П | 39,49 |
|
36 |
Реакции окислительно-восстанови-тельные. Коррозия металлов и способы защиты от нее | 1.4.8 |
2.2.5 2.4.4 |
В | 35,62 |
|
37 |
Реакции, подтверждающие взаимосвязь различных классов неорганических веществ | 2.8 |
2.3.3 2.4.3 |
В | 12,17 |
|
38 |
Реакции, подтверждающие взаимосвязь органических соединений | 3.9 |
2.3.4 2.4.3 |
В | 9,18 |
|
39 |
Расчеты массы (объема, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси), если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества. Расчеты массовой или объемной доли выхода продукта реакции от теоретически возможного. Расчеты массовой доли (массы) химического соединения в смеси |
4.3.5 4.3.6 4.3.8 4.3.9 |
2.5.2 | В | 14,27 |
|
40 |
Нахождение молекулярной формулы вещества | 4.3.7 | 2.5.2 | В | 10,29 |
Всего заданий – 40; из них по уровню сложности: Б – 26; П – 9; В – 5.
Максимальный первичный балл за работу – 64.
Общее время выполнения работы – 180 мин.
Статистика ответов на вопросы ЕГЭ по химии
Задания с кратким ответом
Диаграмма 11
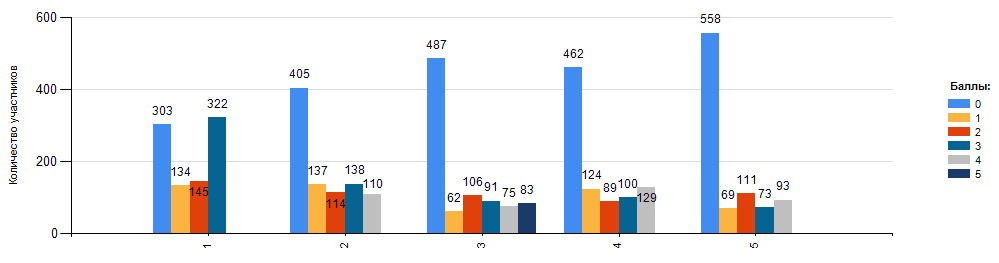
Задания с развернутым ответом
Диаграмма 12
5.Работа региональной предметной комиссии по химии
- Руководитель ПК – Шустов Геннадий Борисович, доктор химических наук, профессор
- Характеристика региональной предметной комиссии (ПК) по химии
Таблица 116
| Эксперты предметной комиссии | Количество |
| Количество экспертов в предметной комиссии, чел. | 36 |
|
из них: - учителей образовательных организаций - преподавателей учреждений высшего профессионального образования - преподавателей учреждений дополнительного профессионального образования |
25 11 - |
|
Из них: - имеющих учёное звание кандидата наук - имеющих учёное звание доктора наук - имеющих звание «Заслуженный учитель РФ» |
6 5 - |
|
Из них - имеющих статус ведущего эксперта - имеющих статус старшего эксперта - имеющих статус основного эксперта |
11 15 10 |
Организация обучения экспертов и работы ПК проходила на базе Института повышения квалификации и переподготовки работников образования Кабардино-Балкарского государственного университета им. Х.М. Бербекова. В целом организация обучения экспертов и работа предметной комиссии по химии прошли на достаточном уровне.
Сведения о согласованности проверки работ экспертами региональной предметной комиссии:
поступило на аппеляцию 252 работ (27,1 % от общего количества работ), удовлетворено 83 аппеляции (8,92 % от общего количества работ); задания или критерии, вызвавшие наибольшие расхождения при проверке работ - нет (0); сведения о результатах федеральных и региональных перепроверок работ – нет (0)
Анализ работ, вызвавших затруднения у экспертов при оценивании – нет работ, вызвавших затруднения экспертов при оценивании.
6.Рекомендации:
Необходимо увеличить практические занятия по изучению генетической взаимосвязи между веществами различных классов (неорганических и (или) органических веществ). По теме: « Составление соответствующих уравнений реакций с учетом условий их проведения с использованием структурных формул органических веществ (для обсуждения)». «Качественные реакции на неорганические вещества и идентификация органических соединений», «Гидролиз солей», «Нахождение молекулярной и структурной формул вещества» и т.д. Организовать на базе института повышения квалификации и переподготовки работников образования Кабардино-Балкарского государственного университета им. Х.М. Бербекова постоянно действующий семинар для учителей химии.
Обсудить результаты ЕГЭ по химии и выявленные в ходе их анализа проблемы во всех школах республики
В критериях необходимо уточнить порядок округления молей при использовании их в расчетных задачах, в вариантах 503, 504, 505, в заданиях 38 имеются опечатки (1 и 2 реакции).
7. Составители отчета о результатах методического анализа:
|
Председатель предметной комиссии |
Шустов Геннадий Борисович, ФГБОУ ВПО «Кабардино-Балкарский государственный университет им. Х.М.Бербекова», профессор, доктор химических наук, профессор |
| Заместитель председателя предметной комиссии | Кузьмичкина Лидия Васильевна, МОУ «Средняя общеобразовательная школа № 14 г.Майский», учитель химии |

 +7 (8662) 42-76-90
+7 (8662) 42-76-90